推荐产品
公司新闻/正文
实例解读文献,一文带你 GET 国自然热点:lncRNA
人阅读 发布时间:2019-08-02 10:45
lncRNA 在近几年科研领域中持续高热不减,研究表明 lncRNA 可通过影响染色质结构和转录因子占位、表观遗传学、以序列和结构特异性结合生物大分子等机制调节基因表达,在发育、机体内平衡和维持细胞命运中发挥重要作用, lncRNA 的异常表达与包括癌症在内的多种疾病密切相关。
随着高通量测序、lncRNA 芯片等技术的发展,越来越多的 lncRNA 被鉴定出来,但具体的作用与功能仍然不是很清楚,因此 lncRNA 的研究领域依然是一片非常广阔的神秘区,具有极大的研究价值。
相关研究往往更受基金资助的青睐,2018 年国自然资助 lncRNA 研究相关项目就高达 717 项。
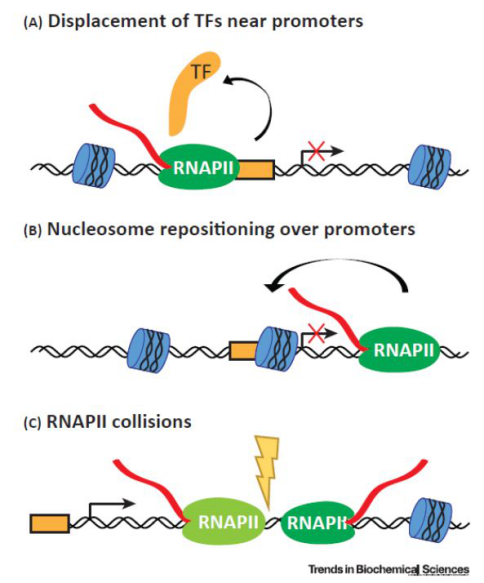
lncRNA 抑制基因转录作用机制

lncRNA 激活基因转录作用机制
※ lncRNA 研究的主要步骤
1.LncRNA 的筛选
常用的方法包括 RNA-seq、lncRNA array 等。通过这些高通量方法,研究人员可快速获得与特定生物学过程或者疾病相关的 lncRNA。
2.LncRNA 的验证
筛选到 lncRNA 后,可通过 NONCODE 或者 lncRNAdb 等网站进一步了解 lncRNA 的相关信息。
在实验方面,可通过定量 PCR 或者 Northern Blot 验证 lncRNA 的表达;通过 RACE 技术获得 lncRNA 全长序列。对于 lncRNA 定位信息,可通过查询 RNAlocate 数据库或者相关分子实验确定。
3.LncRNA 的功能研究
最基本的研究就是构建 lncRNA 表达载体或通过 siRNA、反义核酸等方法沉默 lncRNA,直观地展现 lncRNA 的生物学功能。
在分子机制方面,常常通过 lncRNA 与 RNA、lncRNA 与蛋白、lncRNA 与 DNA 等的相互作用分析来挖掘。
※ 相关文献解读
下面,小编为大家解读一篇 2018 年 10 月发表在 Nature immunology(IF 21.5060)上的文章,希望能给您的 lncRNA 研究提供一点思路和研究方法上的参考。

「活化诱导的 T 淋巴细胞死亡(activation-induced cell death, AICD)可以被癌症利用来逃避免疫破坏。」
这篇文章的研究证明了肿瘤特异性细胞毒性 T 淋巴细胞(CTLs)和 1 型辅助性 T 细胞(TH1),而不是 2 型辅助性 T 细胞和调节性 T 细胞,在乳腺癌和肺癌微环境中对 AICD 敏感。
T 细胞对 AICD 的敏感性通过 lncRNA-- NKILA 抑制 NF-κB 活性进行调节。机制上,T 细胞活化过程中,钙流入(calcium influx)通过 TCR 激活钙调素(Calmodulin),后者使 NKILA 启动子中的乙酰化酶解离,进而导致 STAT1 激活 NKILA 转录。
用 NKILA 基因敲除的 CTLs 处理小鼠能通过增加 CTL 浸润有效抑制乳腺癌患者来源的异种移植物生长。临床上,NKILA 在肿瘤特异性 CTLs 和 TH1 细胞中的过度表达与这些细胞的凋亡和患者更短的生存时间相关。
研究结果突显了 lncRNA 在决定肿瘤介导的 T 细胞 AICD 中的重要性,并提示通过基因操作过继转移 T 细胞中的 lncRNA 可能提供一种新的抗肿瘤免疫疗法。
※ 浅析文章思路
发现疾病表型:研究人员对乳腺癌病人 CTL 进行分析,发现肿瘤浸润 T 细胞亚群对 AICD 有明显的敏感性。

1. 机制研究方面
首先,关联信号通路: 通过转录组谱和基因富集分析(GSEA)发现:NF-κB 失活使活化型 T 细胞对 AICD 敏感(哈哈,又是 NF-κB)。

然后,筛选 lncRNA. 关联的分子/信号通路通过什么途径起作用呢?
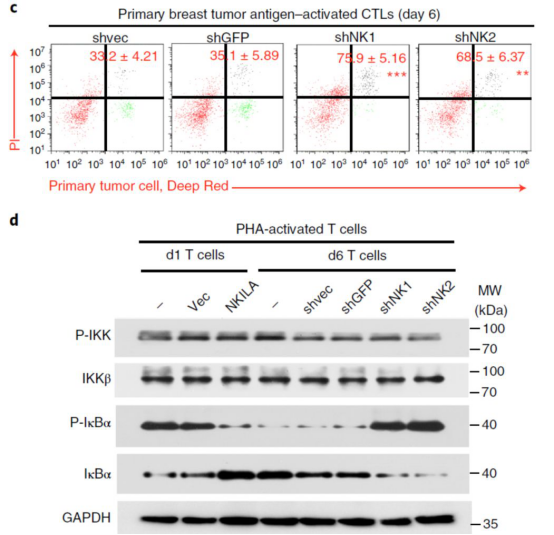
我们的 lncRNA 华丽丽的登场了:通过免疫沉淀(Iκ B 和 p65)和 lncRNA 芯片分析(RIP–chip),筛选到 XLOC_011899, RP11-854K16.3, RP11-315I20.3, NKILA 共 4 个在活化 T 细胞中高表达的 lncRNA,经过 qPCR 验证,shRNA 沉默 T 细胞凋亡分析,最后确定 NKILA。

接下来验证 lncRNA. 先体外细胞验证:通过 shRNA 敲低和过表达,研究 NKILA 对 T 细胞 AICD 和 NF-κB 信号通路的影响。结果显示 NKILA 通过抑制 NF-κB 引起肿瘤特异性 T 细胞发生 AICD。
2. 动物体内验证
采用乳腺癌 PDX 小鼠模型,进一步证明 NKILA 在肿瘤特异性 T 细胞 AICD 中的作用,发现沉默 NKILA 可通过抑制 AICD 改善过继性 T 细胞治疗。

到这里,故事好像已经挺清楚了,但是往往高水平研究高就高在不会止步于此......
※ 临床关联研究
研究人员在乳腺癌和非小细胞肺癌临床肿瘤样本和外周血中进一步研究 NKILA 的表达,发现肿瘤特异性 CTLs 和 TH1 细胞过表达 NKILA,并且过表达 NKILA 的肿瘤特异性 CTLs 和 TH1 细胞对 AICD 敏感。
厉害之处是他们分析了大量乳腺癌和肺癌病人样本,对表达 NKILA 的 CTLs(NKILAhiCTLs)含量与病人的生存期进行了关联分析,发现 NKILAhiCTLs 多,病人预后差。

知其然,还要知其所以然。T 细胞中 NKILA 是怎么被调节的呢?研究人员进一步研究了 T 细胞中 NKILA 的转录机制,通过 GSEA 分析发现 JAK-STAT 调节 NKILA 的表达,并通过报告基因系统找到了 STAT1 结合的 NKILA 启动子区。

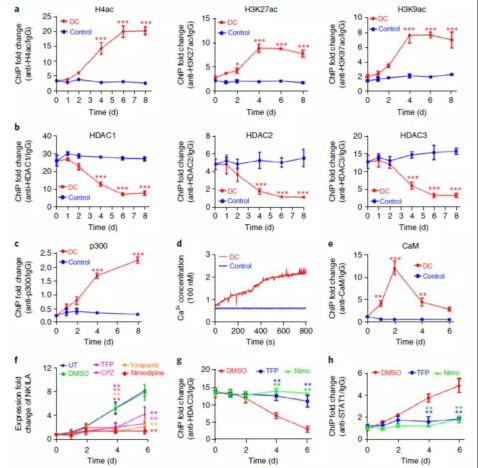
最后,研究人员对 NKILA 启动子区表观遗传调控进行了深入的研究,发现 T 细胞活化过程中,TCR 信号触发钙流入诱导钙调素细胞核移位和活化,活化的钙调素将结合在 NKILA 启动子区域的 HDACs 移除并打开染色质,便于 STAT1 结合并激活 NKILA 的转录。
文献就为大家解读到这里,感兴趣的朋友建议查阅原文献。
※ 参考文献
1) Huang D, et al. NKILA lncRNA promotes tumor immune evasion by sensitizing T cells to activation-induced cell death. Nat Immunol. 2018;19(10):1112-1125.
2) Kaikkonen MU, Adelman K. Emerging Roles of Non-Coding RNA Transcription. Trends Biochem Sci. 2018 Sep;43(9):654-667.
随着高通量测序、lncRNA 芯片等技术的发展,越来越多的 lncRNA 被鉴定出来,但具体的作用与功能仍然不是很清楚,因此 lncRNA 的研究领域依然是一片非常广阔的神秘区,具有极大的研究价值。
相关研究往往更受基金资助的青睐,2018 年国自然资助 lncRNA 研究相关项目就高达 717 项。

lncRNA 抑制基因转录作用机制

lncRNA 激活基因转录作用机制
※ lncRNA 研究的主要步骤
1.LncRNA 的筛选
常用的方法包括 RNA-seq、lncRNA array 等。通过这些高通量方法,研究人员可快速获得与特定生物学过程或者疾病相关的 lncRNA。
2.LncRNA 的验证
筛选到 lncRNA 后,可通过 NONCODE 或者 lncRNAdb 等网站进一步了解 lncRNA 的相关信息。
在实验方面,可通过定量 PCR 或者 Northern Blot 验证 lncRNA 的表达;通过 RACE 技术获得 lncRNA 全长序列。对于 lncRNA 定位信息,可通过查询 RNAlocate 数据库或者相关分子实验确定。
3.LncRNA 的功能研究
最基本的研究就是构建 lncRNA 表达载体或通过 siRNA、反义核酸等方法沉默 lncRNA,直观地展现 lncRNA 的生物学功能。
在分子机制方面,常常通过 lncRNA 与 RNA、lncRNA 与蛋白、lncRNA 与 DNA 等的相互作用分析来挖掘。
※ 相关文献解读
下面,小编为大家解读一篇 2018 年 10 月发表在 Nature immunology(IF 21.5060)上的文章,希望能给您的 lncRNA 研究提供一点思路和研究方法上的参考。

「活化诱导的 T 淋巴细胞死亡(activation-induced cell death, AICD)可以被癌症利用来逃避免疫破坏。」
这篇文章的研究证明了肿瘤特异性细胞毒性 T 淋巴细胞(CTLs)和 1 型辅助性 T 细胞(TH1),而不是 2 型辅助性 T 细胞和调节性 T 细胞,在乳腺癌和肺癌微环境中对 AICD 敏感。
T 细胞对 AICD 的敏感性通过 lncRNA-- NKILA 抑制 NF-κB 活性进行调节。机制上,T 细胞活化过程中,钙流入(calcium influx)通过 TCR 激活钙调素(Calmodulin),后者使 NKILA 启动子中的乙酰化酶解离,进而导致 STAT1 激活 NKILA 转录。
用 NKILA 基因敲除的 CTLs 处理小鼠能通过增加 CTL 浸润有效抑制乳腺癌患者来源的异种移植物生长。临床上,NKILA 在肿瘤特异性 CTLs 和 TH1 细胞中的过度表达与这些细胞的凋亡和患者更短的生存时间相关。
研究结果突显了 lncRNA 在决定肿瘤介导的 T 细胞 AICD 中的重要性,并提示通过基因操作过继转移 T 细胞中的 lncRNA 可能提供一种新的抗肿瘤免疫疗法。
※ 浅析文章思路
发现疾病表型:研究人员对乳腺癌病人 CTL 进行分析,发现肿瘤浸润 T 细胞亚群对 AICD 有明显的敏感性。

1. 机制研究方面
首先,关联信号通路: 通过转录组谱和基因富集分析(GSEA)发现:NF-κB 失活使活化型 T 细胞对 AICD 敏感(哈哈,又是 NF-κB)。

然后,筛选 lncRNA. 关联的分子/信号通路通过什么途径起作用呢?
我们的 lncRNA 华丽丽的登场了:通过免疫沉淀(Iκ B 和 p65)和 lncRNA 芯片分析(RIP–chip),筛选到 XLOC_011899, RP11-854K16.3, RP11-315I20.3, NKILA 共 4 个在活化 T 细胞中高表达的 lncRNA,经过 qPCR 验证,shRNA 沉默 T 细胞凋亡分析,最后确定 NKILA。

接下来验证 lncRNA. 先体外细胞验证:通过 shRNA 敲低和过表达,研究 NKILA 对 T 细胞 AICD 和 NF-κB 信号通路的影响。结果显示 NKILA 通过抑制 NF-κB 引起肿瘤特异性 T 细胞发生 AICD。

2. 动物体内验证
采用乳腺癌 PDX 小鼠模型,进一步证明 NKILA 在肿瘤特异性 T 细胞 AICD 中的作用,发现沉默 NKILA 可通过抑制 AICD 改善过继性 T 细胞治疗。

到这里,故事好像已经挺清楚了,但是往往高水平研究高就高在不会止步于此......
※ 临床关联研究
研究人员在乳腺癌和非小细胞肺癌临床肿瘤样本和外周血中进一步研究 NKILA 的表达,发现肿瘤特异性 CTLs 和 TH1 细胞过表达 NKILA,并且过表达 NKILA 的肿瘤特异性 CTLs 和 TH1 细胞对 AICD 敏感。
厉害之处是他们分析了大量乳腺癌和肺癌病人样本,对表达 NKILA 的 CTLs(NKILAhiCTLs)含量与病人的生存期进行了关联分析,发现 NKILAhiCTLs 多,病人预后差。

知其然,还要知其所以然。T 细胞中 NKILA 是怎么被调节的呢?研究人员进一步研究了 T 细胞中 NKILA 的转录机制,通过 GSEA 分析发现 JAK-STAT 调节 NKILA 的表达,并通过报告基因系统找到了 STAT1 结合的 NKILA 启动子区。

最后,研究人员对 NKILA 启动子区表观遗传调控进行了深入的研究,发现 T 细胞活化过程中,TCR 信号触发钙流入诱导钙调素细胞核移位和活化,活化的钙调素将结合在 NKILA 启动子区域的 HDACs 移除并打开染色质,便于 STAT1 结合并激活 NKILA 的转录。

文献就为大家解读到这里,感兴趣的朋友建议查阅原文献。
※ 参考文献
1) Huang D, et al. NKILA lncRNA promotes tumor immune evasion by sensitizing T cells to activation-induced cell death. Nat Immunol. 2018;19(10):1112-1125.
2) Kaikkonen MU, Adelman K. Emerging Roles of Non-Coding RNA Transcription. Trends Biochem Sci. 2018 Sep;43(9):654-667.